Q3. 先発医薬品との治療効果の差は?
厚生労働省が定める基準によると、生物学的同等性試験の許容域を80%~125%としているが、これはすなわち、ジェネリック医薬品と先発医薬品の治療効果が最大45%の範囲で異なるということを示しているのか。
実際に承認されている医薬品のデータの検証を実施したところ、先発医薬品とジェネリック医薬品の血中濃度にはほとんど差がありませんでした。
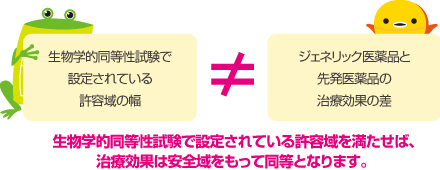
生物学的同等性試験の許容域は、ジェネリック医薬品と先発医薬品の血中濃度の比の幅を示しているのであって、治療効果そのものの差の幅を示しているわけではありません。通常、医薬品の効果や副作用は有効成分の血中濃度に従って発現しますので、生物学的同等性試験の許容域内であれば、治療効果は同等であると考えられます。
血中濃度に関しては、同じ人が同じ医薬品を服用した場合であっても、服用する人の体質や体調等が医薬品の吸収、代謝及び排泄に影響を及ぼすなど、除外できない自然のばらつきが常に起こり得ます。生物学的同等性試験の許容域は、このような血中濃度のばらつき等を考慮したうえで、ジェネリック医薬品と先発医薬品の治療効果が同等と評価できる幅を、安全域を含めて設定しています(※5)。
実際に、PMDAが発足した2004年4月1日~2011年1月15日までに承認された経口製剤のジェネリック医薬品について実施された930件の生物学的同等性試験について、ジェネリック医薬品と先発医薬品の差の検証が行われました。これは、その期聞において上記に示す品目全体の約8割に当たります。

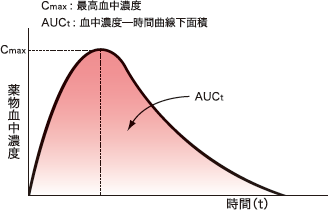
ジェネリック医薬品と先発医薬品における血中濃度の平均的な差を比較するために、生物学的同等性試験の評価パラメーターである最高血中濃度(Cmax)及び血中濃度一時間曲線下面積(AUCt)を用いて検証を行いました。それぞれのパラメーターの差を先発医薬品に対する比で表して、930試験について平均すると、Cmaxについては4.6%、AUCtについては3.9%となり、ジェネリック医薬品と先発医薬品の差はほとんどないという結果になりました(図表1参照)。
このことからも、生物学的同等性試験の許容域を、単純にジェネリック医薬品と先発医薬品の治療効果の差と置き換えることは誤りであることが理解できると思います。
| パラメーター | 試験数 | ジェネリック医薬品と先発医薬品の差 注1 (%) | 先発医薬品に対するジェネリック医薬品の比 注2 |
|---|---|---|---|
| Cmax | 930 | 4.61 ± 3.41 | 1.00 ± 0.06 |
| AUCt | 930 | 3.87 ± 2.98 | 1.00 ± 0.05 |
注1 ((ジェネリック医薬品-先発医薬品)/先発医薬品)の百分率の絶対値(平均値±標準偏差)
注2 対数値の平均値の差から計算したパラメーター値の比(平均値±標準偏差)
(※5)
生物学的同等性試験の許容域は、先発医薬品とジェネリック医薬品の比を1と仮定した場合に、先発医薬品とジェネリック医薬品の血中濃度における平均値の比の統計的な幅(信頼区間)が100%を中心として±20%(対数変換を行う場合は80%~125%)内にあることを意味し、ジェネリック医薬品と先発医薬品が最大45%異なり得るということを意味しているわけではありません。仮に、ジェネリック医薬品と先発医薬品の血中濃度の平均値に45%の差がある場合、それらの比が生物学的同等性の許容域に収まることはありません。なお、対数変換を行う場合、信頼区間の上側限界が125%とされていますが、これは、対数変換して統計処理を行うことを考慮したものであり、対数変換しない場合に比べて許容域が広いことを意味するものではありません。
「ジェネリック医薬品への疑問に答えます ~ジェネリック医薬品Q&A~(厚生労働省:平成27年2月版)![]() 」をもとにニプロESファーマ株式会社作成
」をもとにニプロESファーマ株式会社作成
当サイトに含まれている文書・写真・イラスト等の利用については、ご利用規約をご覧ください。